市販生培地の精度管理のいろは
~使用者のための~
済生会茨木病院 谷本理香
去る5月18日,日本ベクトン・ディッキンソン株式会社の大川三郎先生を講師にお迎えして御講演頂きました。精度管理といえば検査技術の評価となっていますが,正しく管理された培地や試薬を使用することが必要です。培地や試薬の品質管理・精度管理についてどのようなものなのか,何を管理するのかについて御講演頂きました。
①NCCLS M22-2Aの概要(現在の米国での標準法)
・ 本規格は1990年発行の認定規格の改訂版である。
・ M22-Aはユーザー及びメーカーに市販生培地の品質保証手順を提供する。
・ 本規格では不合格率が極めて低く,確立された培地はユーザー自身による再試験を必要としないことを基本前提としている。
・ メーカーが市販培地の性能を評価できる方法も提供する。
②イントロダクション
・ CAP(College of American Pathologist)により35タイプの市販生培地を評価した。
・ 35万ロット,6700万枚(または本)の平板,試験管,ボトル培地が試験された。
・ 不良率の高い製品はカンピロバクター培地(0.388%),サイア・マーチン寒天培地(0.31%)
・ 0.1%以上の不良率を示した培地は5製品のみであった。(SS 寒天,EMB寒天,コロンビアCNA・チョコレート寒天培地・サブロー寒天培地)
*生培地の性能的欠陥品の検出にかかるコスト
目視観察・pH・発育支持能試験→1ロット 平均$3
性能的欠陥率が3%以下の培地についてはユーザー自身の試験が排除できれば,
医療効果の疑わしい大きな出費を回避できる。
③製造会社がするべき試験
・ 精度管理菌株の入手-American Type Culture Collection(ATCC)及びATCC由来市販培養株
・ 精度管理菌株の維持-コロニーの形態などから純度を確認後,50-100mlの凍結保護培地(10-15%のグリセロールを含む,TSBまたは脱繊維処理ヒツジ血,ウサギ血,スキムミルク)に懸濁する。凍結培地からの接種する場合は,凍結する前に懸濁液を0.5マックファーランド(N.gonorrheaはNo.1マックファーランド)に調整する。(-70℃以下では半永久的,-50℃~-70℃では1年間,-50℃より高い温度では保存すべきではない)
・ 凍結保存菌株の調製
・ 標準菌株の使用法-凍結保存培養菌からは最高3回まで継代培養してよい。3回以上継代培養すると,表現型が変化する危険性がある。
・ 精度管理のための試験法
非選択培地-#0.5菌液を100倍希釈し,10μlを画線接種
選択培地――#0.5菌液を10倍希釈し,10μlを画線接種
・ 結果の解釈
・ 使用者へのデータの報告
1.メーカーは性能試験から製品がNCCLSM22-A2に合格していることが証明されたことをラベル,添付文書,マニュアル,あるいはその他文書の形で示さなければならない。
2.メーカーはまた,実施した追加試験,無菌試験,ph測定についても表示しなければならない。
*表に記載されていない培地
1.メーカーはユーザーに対し,①使用した菌株②ph③評価性能基準④試験菌の反応⑤汚染の評価 を含めた品質管理法を知らさねばならない。
2.表に揚載されていない培地についてはユーザー自身が性能試験を行わなければならない。
・ 製品の輸送と保存
1.培地は過度に湿気を失わないよう,そして機械的及び熱保護手段を備えた形で輸送しなければならない。
2.有効期限は培地性能評価に基ずくものであり,評価結果はメーカーが保管する。
3.有効期限を確定する際には輸送および保管の条件も考慮する。
製造会社の市販生培地品質管理法
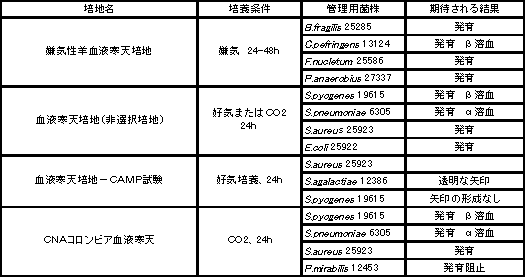
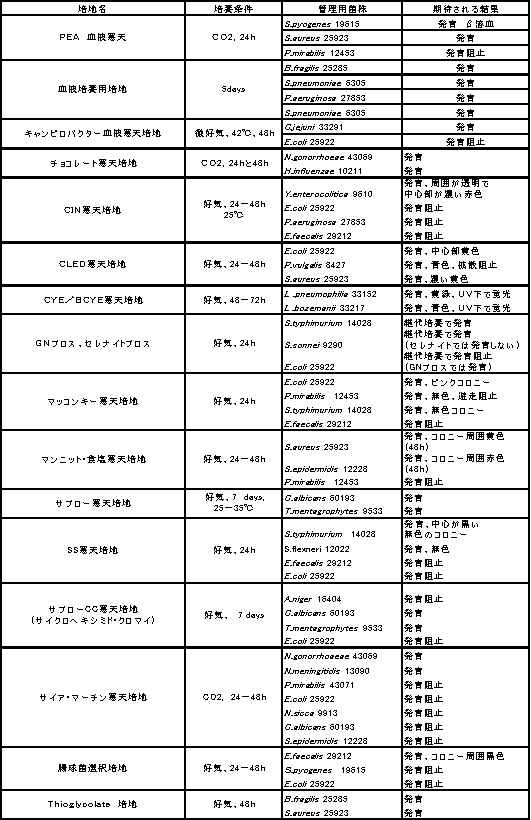
④使用者が行う試験
1.表に掲載のない培地
性能試験
・ ユーザーにより調整された微生物培地は全て,試験に関しては確立された規制の要件を満たさなければならない。市販の調製済み培地のユーザーは,今後も表に掲載されていない培地は,ユーザーで性能試験を実施しなければならない。
・ 非商業的に関係施設に培地を供給している施設から培地を得ているユーザーも,市販の調製済み培地を対象とした本規格に記載されているガイドラインに従わなければならない。製造者(培地を調製している検査所)は,商業目的のメーカーを対象に推奨されている品質保証基準と同じ基準を適用しなければならない。このような書類が提供されない場合には,供給を受けているユーザーはこれら培地を自らが調製する場合と同様にして試験しなければならない。
2.カンピロバクター選択培地
3 .病原性ナイセリア用選択培地(サイアーマーチン培地など)
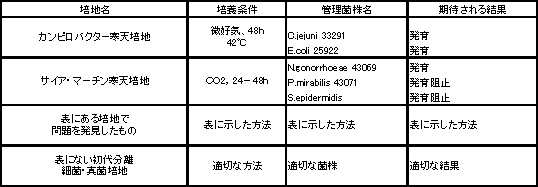
4.その他の品質保証基準
培地に欠陥が見つかった場合には,検査室はその観察結果を書面にし,メーカーに通知しなければならない。このような欠陥としては,増殖の不良あるいは期待されるコロニーサイズにならないこと,汚染の兆候,乾燥またはひび割れが挙げられる。メーカーと共に適切は是正処置を確立して,それを検査室の記録に残さなければならない。メーカーがその欠陥を納得するまでは,この様な作業が培地の交換につながらないこともある。この様な場合,欠陥の原因が特定され,是正されるまでは,ユーザーによる培地の追加試験が必要となる。
血液寒天培地(TSAⅡ5%ヒツジ血液寒天培地)

≪ガゼインペプトン≫
・ カゼインをトリプシンまたは膵消化したもの。
・ タンパクとしての栄養的にすぐれ,安価であり,最もよく使用される。
・ トリプトファン含有量が多いが,シスチン,メチオニンのような硫黄(S)を含むアミノ酸が少ない。
・ インドール試験には好適であるが,硫化水素産生試験用には不適。
≪大豆ペプトン≫大豆をパパインで消化したもの。
・ 植物組織の炭水化物とビタミンとくにチアミン(B1)が豊富
・ ナイセリア・ブルセラ・などの栄養要求が厳しい菌についても強い発育支持力。
・ ペプトン・寒天に含まれる菌の発育阻害物質の作用を中和する効果が顕著
・ エキス類のかわりに他のペプトンと併用
血液寒天培地の条件